2. 青岛海洋科学与技术国家实验室 海洋渔业科学与食物产出过程功能实验室 青岛 266071;
3. 大连海洋大学 大连 116023
2. Laboratory for Marine Fisheries Science and Food Production Processes, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266071;
3. Dalian Ocean University, Dalian 116023
孕酮受体膜组分1 (Progesterone receptor membrane component 1, PGRMC1)为广泛存在于真核生物中的膜相关的孕激素受体蛋白(Membrane-associated progesterone receptor protein, MAPR)家族中的一员。PGRMC1以多肽单体的形式存在,为二聚体或低聚体,这些存在形式均可以介导孕激素快速反应性,引起膜相关信号传导(张颖等, 2013)。研究发现,在不同的环境条件下PGRMC1能改变它的亚细胞定位,参与不同的细胞调控活动;与PGRMC1蛋白的多亚细胞定位特点对应的是PGRMC1能与不同的蛋白结合,通过不同的配基相互作用发挥不同的生物学功能(Lösel et al, 2008)。已有研究表明,PGRMC1在参与大鼠(Rattus norvegicus)和人(Homo sapiens)颗粒/黄体细胞胆固醇代谢和类固醇生物合成(Hughes et al, 2007; Suchanek et al, 2005)、基因转录(Peluso et al, 2012)、介导孕激素在卵巢细胞中的抗凋亡活动(Mansouri et al, 2008)、诱导卵母细胞成熟(Peluso et al, 2008)、促进体外卵巢细胞的存活(Luciano et al, 2008)、细胞分裂(Luciano et al, 2011; Liu et al, 2009)和精子顶体反应(Bryan et al, 2015)等方面有重要的调控作用。
目前,在鱼类中关于PGRMC1的相关研究较少,仅在虹鳟(Oncorhynchus mykiss)(Mourot et al, 2006)、斜带石斑鱼(Epinephelus coioides)(徐驰, 2011)1)、海七鳃鳗(Petromyzon marinus)(Bryan et al, 2015)有过报道。PGRMC1在鲆鲽类中的繁殖调控作用机制尚不清楚,相关研究亟待开展。本实验室前期实验初步研究了半滑舌鳎(Cynoglossus semilaevis) PGMRC1基因结构及表达特征(张金勇等, 2016),本研究采用原位杂交、免疫组化技术和Western blotting等方法研究了半滑舌鳎PGRMC1基因在半滑舌鳎不同组织中的细胞学定位和表达特征,为探明PGRMC1的生理功能,特别是在下丘脑-垂体-性腺轴(HPG轴)和卵母细胞成熟过程中所参与的调控作用提供基础资料。
1) Xu C. mPRα and PGRMC1: cDNAs cloning and expression profiles in orange-spotted grouper, Epinephelus coioides. Master's Thesis of Sun Yat-sen University, 2011 [徐驰.斜带石斑鱼mPRα和PGMRC1基因cDNA的克隆及表达模式分析.中山大学硕士研究生学位论文, 2011]
1 材料与方法 1.1 实验材料实验所用半滑舌鳎取自山东烟台黄海水产有限公司。挑取人工培育达到性成熟3龄雌性亲鱼21尾。所用亲鱼全长为52-59 cm,体重为1183.9-1349.2 g。实验用鱼的培育条件:在室内水泥池中(5 m×5 m×1 m)全年开放流水培育,饲喂人工配合饲料,水温为10-25℃,盐度为27-31, pH 7.8-8.4, 溶解氧为5 mg/L以上。使用MS-222麻醉亲鱼后解剖,留取脑、垂体、性腺、肾等各组织样品,4%多聚甲醛[溶于0.01 mol/L磷酸盐缓冲液(PBS)中]在4℃条件下固定20 h,梯度甲醇脱水,-20℃保存在甲醇中的样品,一部分用于免疫组化,一部分样品用于原位杂交;液氮速冻后转至-80℃保存各组织样品,用于总蛋白的提取。
1.2 PGRMC1/pBST-18质粒构建和探针制备根据所得半滑舌鳎PGRMC1的cDNA序列全长,设计扩增产物为280 bp的原位杂交探针引物,PGRMC1-ISH-F (5′-AAGCTTCCGAGGAAAGCGAAGTAAC-3′)和PGRMC1-ISH-R (5′-GAATTCCATAAAACTTCTTCCCCCG-3′),构建重组质粒(PGRMC1/pBST-18, Roche)作为模板制备地高辛标记的RNA探针,将扩增后的阳性菌落提取的质粒分别用限制性内切酶Hind Ⅲ和EcoR Ⅰ酶切,使其线性化,按照Roche公司的DIG RNA Labeling Kit (SP6/T7)试剂盒说明书,分别用SP6、T7转录酶进行体外转录,反应体系为10 μl:线性化质粒DNA 4 μg,DIG-UTP Mixture 1 μl, 10×Buffer 1 μl,反转录酶1 μl,RNA酶抑制剂1 μl,合成地高辛标记的正、反义RNA探针。合成的RNA探针用1%琼脂糖电泳和紫外分光光度计鉴定检测。
1.3 切片原位杂交分析将处理好的原位杂交切片在烘箱37℃烘3 h后进行切片原位杂交,二甲苯脱蜡处理3次(每次5 min),乙醇梯度脱水(100%乙醇2次,每次10 min;95%、70%、50%乙醇各1次,每次5 min)。4% PFA-PBS固定10 min。PBS冲洗3次,每次10 min。0.2 mol/L的HCl处理10 min。PBST洗涤3次,每次10 min。10 μg/ml蛋白酶K消化10 min。PBST洗涤3次,每次5 min。加入含tRNA和肝素预杂交液,70℃预杂交8 h,再加入反义RNA探针200 ng的杂交液,70℃过夜。50%无tRNA及肝素的预杂交液和50% 2×SSC,70℃放置15 min;0.2×SSC,70℃放置1 h。1×MAB室温5 min。含10%山羊血清的封闭液室温封闭6 h。1:500稀释的碱性磷酸酶标记的抗地高辛抗体,4℃孵育过夜。PBST室温冲洗6次,每次15 min;碱性磷酸缓冲液室温2次,每次10 min。加200 μl BCIP/NBT底物溶液,置黑暗处显色,观察颜色变化。待显色达到理想着色后,PBST洗涤5次,每次5 min,终止反应,4% PFA-PBS固定10 min,PBST洗3次,每次5 min;酒精梯度脱水,二甲苯透明,封片,拍照。
1.4 Western blotting取冻存的半滑舌鳎脑、垂体、卵巢等组织(约100 mg),加入1 ml动物组织蛋白提取试剂,匀浆器充分匀浆、冰浴静置30 min,于4℃、12000 r/min离心30 min,取上清液,即得到组织蛋白提取液。12% SDS-PAGE电泳检测提取蛋白的质量,并使用蛋白测定试剂盒测定组织总蛋白浓度。
分析半滑舌鳎PGRMC1蛋白序列选择抗原表位,制备抗体。统一蛋白上样量为40 μg,12% SDS-PAGE胶蛋白电泳,60 V 1 h,然后90 V 1.5 h;经转膜、PVDF膜活化,按阳极-滤纸-PVDF膜-凝胶-滤纸-阴极的顺序放入半干式转膜仪,400 mA 25 min将分子量标准和凝胶上的蛋白电转移到PVDF膜上;1×PBST洗涤PVDF膜2次,每次5 min,5%脱脂奶粉溶液封闭(1×PBST稀释)室温3 h;洗涤;加一抗(半滑舌鳎PGRMC1多克隆抗体)与5% BSA室温摇床2 h,一抗稀释1:1500 (1×PBST稀释);二抗(羊抗兔IgG抗体)室温摇床2 h,稀释度为1:2000 (1×PBST稀释)。DAB显色,Nikon E80i显微镜拍照,蛋白灰度分析。同时采用空白对照检测多克隆抗体的特异性。
1.5 免疫组化取100%甲醇中保存的样品,使用常规切片制备方法获取免疫组化切片,免疫组化实验过程:二甲苯脱蜡2次,每次5 min;梯度乙醇复水3 min;1×PBST洗涤;3% H2O2封闭内源酶,室温孵育15 min;PBST洗涤;0.01 mol/L柠檬酸盐缓冲液修复抗原,微波炉加热沸腾后,中低档保持95℃ 20 min,自然冷却至室温;PBST洗涤;5% BSA封闭(溶于1×PBST)室温摇床2 h;半滑舌鳎PGRMC1抗体(1:1000)稀释,使其完全覆盖组织切片,湿盒中室温过夜;PBST洗涤;二抗使用羊抗兔IgG抗体(1:1000稀释),湿盒中室温1 h;PBST洗涤;DAB显色;PBST洗涤;苏木精染液复染3-5 min;0.1% HCl分化复蓝后立即自来水冲洗;梯度乙醇脱水;二甲苯透明2 min;封片;Nikon E80i显微镜拍照。阴性对照组采用1×PBS代替一抗,孵育方法相同。
1.6 统计分析蛋白表达数据使用SPSS 17.0软件进行单因素方差分析(One-way ANOVA)检验和Duncan’s多重比较分析。相对表达量数据均以平均数±标准误(Mean±SE)表示,当P < 0.05时表示差异显著,AIC.AlphaView成像分析系统(Cell Biosciences Inc)分析蛋白灰度,并制成柱状图。
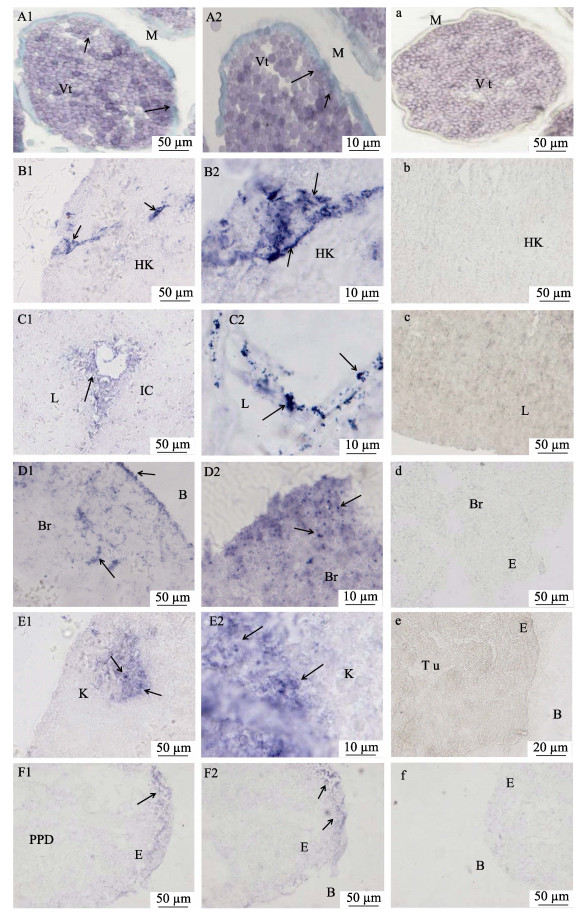
2 结果 2.1 PGRMC1基因的细胞学定位原位杂交分析PGRMC1 mRNA在繁殖相关组织中的细胞学定位见图 1。图 1-A1显示,在成熟卵巢组织中,PGRMC1 mRNA在卵母细胞膜上显著性表达,图 1-A2为放大1000倍表达结果,明显看出在卵母细胞膜上的阳性信号。图 1-B1显示在头肾组织中,PGRMC1 mRNA的表达在组织外周的显色更显著,并向内管道式延伸,图 1-B2为放大1000倍结果,明显显示PGRMC1 mRNA表达部位并向内管道式延伸。图 1-C1显示肝脏PGRMC1 mRNA主要定位在胆小管周围,图 1-C2为放大1000倍结果。图 1-D1显示,在脑组织中,PGRMC1 mRNA主要定位在外周部位,图 1-D2为部分放大区域。图 1-E1及放大1000倍的图 1-E2显示,PGRMC1 mRNA在肾小管区域显色信号丰富。图 1-F1和图 1-F2显示,在垂体组织中,PGRMC1 mRNA阳性信号分布于分散的垂体细胞中。
|
图 1 半滑舌鳎PGRMC1在不同组织中的定位 Figure 1 Location of PGRMC1 gene in different tissues of C. semilaevis A1:卵巢; B1:头肾; C1:肝脏; D1:脑; E1:肾; F1:垂体; A2、B2、C2、D2和E2分别为卵巢、头肾、肝脏、脑和肾放大1000倍,F2为垂体放大200倍; a、b、c、d、e和f:卵巢、头肾、肝脏、脑、肾和垂体的阴性对照组TU:肾小管; K:肾脏细胞; Vt:卵黄; E:组织边缘; L:肝脏细胞; B:空白区; Br:脑细胞; HK:头肾细胞; M:卵母细胞膜; P:垂体细胞; PPD:外周部位 A1: Ovary; B1: Head-kidney; C1: Liver; D1: Brain; E1: Kidney; F1: Pituitary; A2, B2, C2, D2 and E2: Ovary, head-kidney, liver, brain, and kidney (×1000); F2: Pituitary (×200); a, b, c, d, e, and f: Negative control of ovary, head-kidney, liver, brain, kidney, and pituitary TU: Tubules; K: Kidney; Vt: Vitelo genic oocytes; E: Edge of tissues; L: Liver; B: Blank; Br: Brain cell; HK: Head-kidney cell; M: Oocyte membrane; PPD: Proximal part distalis |
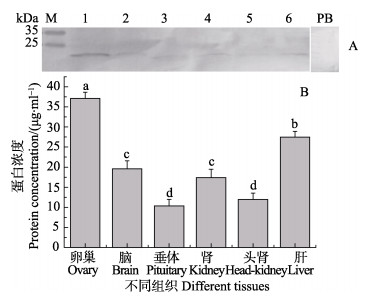
半滑舌鳎PGRMC1蛋白在不同组织表达水平的结果显示,在卵巢、脑、垂体、肝脏、头肾和肾脏组织检测到蛋白条带,分子量约为21 kDa,与预测的蛋白分子量20.64 kDa相当(图 2-A)。对照组采用多肽抗原进行Western blotting,证实了抗体特异性。半滑舌鳎PGRMC1蛋白表达量在卵巢、脑、肝脏中相对较高,在肾脏、垂体、头肾组织中也有表达,但表达量相对较少(图 2-B)。基于PGRMC1蛋白在卵巢、脑和肝脏等组织中的较高水平表达,说明PGRMC1在半滑舌鳎多种组织中参与调节孕激素生理功能。
|
图 2 半滑舌鳎各组织PGRMC1蛋白表达量 Figure 2 Expression of PGRMC1 protein in the tissues of C. semilaevis A: PGRMC1蛋白表达电泳; B: PGRMC1蛋白表达量化丰度1:卵巢; 2:脑; 3:垂体; 4:肾; 5:头肾; 6:肝; M:蛋白分子量标准; PB:阴性对照不同字母间差异显著(P < 0.05) A: Electrophoregram of PGRMC1 protein expression; B: Protein expression abundance for PGRMC1 1: Ovary; 2: Brain; 3: Pituitary; 4: Kidney; 5: Head-kidney; 6: Liver; M: Protein molecular weight marker; PB: Negative control Different letters represent significant difference (P < 0.05) |
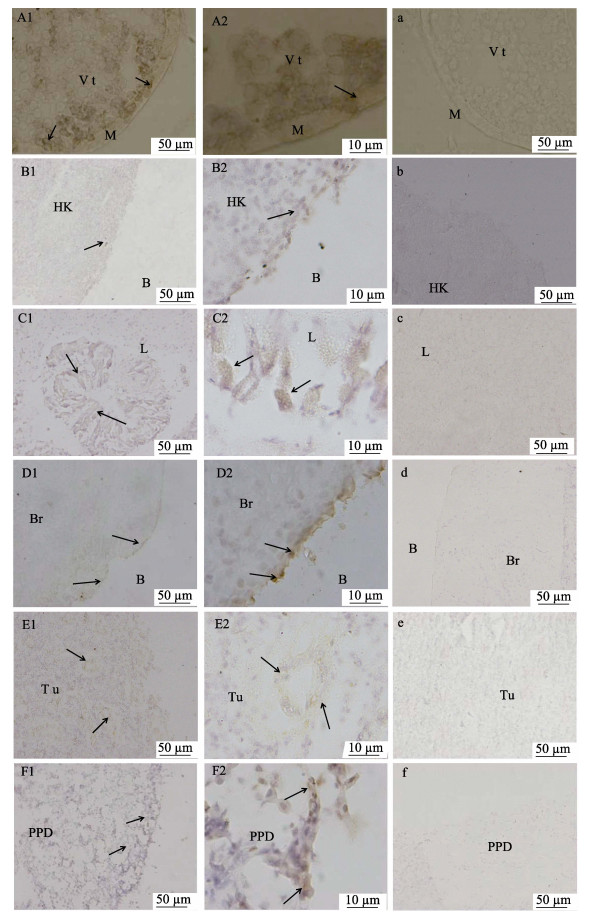
免疫组化结果表明,半滑舌鳎PGRMC1在卵巢、脑和垂体的细胞学定位与原位杂交实验结果基本一致(图 3)。PGRMC1在性成熟半滑舌鳎不同组织中的分布强度见表 1。图 3-A1结果显示,在性成熟卵巢组织中,PGRMC1主要在卵母细胞膜上表达丰富,放大1000倍的图 3-A2可以很明显地看出其在膜附近的表达。图 3-B1结果显示,头肾的表达部位主要在外周组织,放大1000倍的图 3-B2可以很明显地看出其在外周部位的表达。图 3-C1显示肝脏PGRMC1主要定位在肝静脉周围显色,放大1000倍的图 3-C2可以看出PGRMC1在肝静脉管腔内外部位表达。在显示脑组织的图 3-D1中,PGRMC1主要定位在脑组织的神经元,图 3-D2为放大1000倍表达结果。图 3-E1显示,在肾脏组织中,PGRMC1主要在外周组织和肾小管区域中表达,右图 3-E2为放大1000倍结果,很明显地看出其在外周部位以及肾小管的管腔内外表达。图 3-F1和图 3-F2显示,在垂体组织,PGRMC1主要分布在垂体中分散的细胞。
|
图 3 半滑舌鳎PGRMC1蛋白在不同组织中的分布 Figure 3 Location of PGRMC1 protein in different tissues of C. semilaevis A1:卵巢; B1:头肾; C1:肝脏; D1:脑; E1:肾; F1:垂体; A2、B2、C2、D2、E2和F2:卵巢、头肾、肝脏、脑、肾和垂体放大1000倍; a、b、c、d、e和f:卵巢、头肾、肝脏、脑、肾和垂体的阴性对照组TU:肾小管; K:肾脏细胞; Vt:卵黄; E:组织边缘; L:肝脏细胞; B:空白区; Br:脑细胞; HK:头肾细胞; M:卵母细胞膜; P:垂体细胞; PPD:外周部位 A1: Ovary; B1: Head-kidney; C1: Liver; D1: Brain; E1: Kidney; F1: Pituitary; A2, B2, C2, D2, E2 and F2: Ovary, head-kidney, liver, brain, kidney, and pituitary (×1000); a, b, c, d, e, and f: Negative control of ovary, head-kidney, liver, brain, kidney, and pituitary. TU: Tubules; K: Kidney; Vt: Vitelo genic oocytes; E: Edge of tissues; L: Liver; B: Blank; Br: Brain cell; HK: Head-kidney cell; M: Oocyte membrane; PPD: Proximal part distalis |
|
|
表 1 PGRMC1在性成熟半滑舌鳎组织中的分布强度 Table 1 Intensity distribution of PGRMC1 in different tissues of C. semilaevis |
PGRMC1在大鼠和人颗粒/黄体细胞胆固醇代谢和性类固醇生物合成(Hughes et al, 2007; Suchanek et al, 2005), 介导孕激素在卵巢细胞中的抗凋亡和正向调控具有催化活性的芳香化酶家族基因(Mansouri et al, 2008),诱导哺乳动物卵母细胞成熟(Peluso et al, 2008)和精子顶体反应(Bryan et al, 2015)等方面有重要的调控作用。前期研究已克隆得到半滑舌鳎PGRMC1基因全长序列,并对PGRMC1 mRNA在性成熟雌性半滑舌鳎不同组织的表达特征进行了分析,发现半滑舌鳎PGMRC1 mRNA组织表达广泛,其中卵巢组织中相对表达量最高(张金勇等, 2016)。
本研究通过Western blotting检测PGRMC1蛋白在半滑舌鳎不同组织的表达水平,显示PGRMC1蛋白在卵巢、脑、肝脏中表达量相对较高,而在垂体、肾和头肾组织中也有一定的表达。免疫组化和RNA原位杂交实验结果显示,PGRMC1蛋白和mRNA阳性信号在性成熟卵巢的卵母细胞膜上、脑内部分神经元区域和垂体内分散的细胞上有明显分布。这进一步揭示PGRMC1在性成熟雌性半滑舌鳎不同组织的表达特征,即PGRMC1较丰富地表达于卵巢、脑和肝脏,说明PGRMC1在半滑舌鳎繁殖轴和肝脏组织介导孕激素参与繁殖内分泌调控。原位杂交检测斑节对虾(Penaeus monodon)卵巢组织中PGRMC1 mRNA的杂交信号,发现在卵巢卵黄形成早期和卵黄形成期都有杂交信号,并且在卵黄形成期,卵巢比卵黄形成早期卵巢的杂交信号明显;免疫组化显示,PGRMC1蛋白阳性信号也存在于卵泡层和滤泡细胞细胞膜(Preechaphol et al, 2010);这些研究结果表明,PGRMC1在斑节对虾卵母细胞成熟过程中起着重要的调控作用。Mourot等(2006)采用原位杂交方法检测到未性成熟的虹鳟鱼卵巢组织PGRMC1 mRNA的杂交信号;在牛(Bovine)的卵母细胞,qRT-PCR研究发现,PGMRC1 mRNA表达丰富(Dode et al, 2006);前期的研究表明,在半滑舌鳎繁殖周期,卵巢中PGRMC1 mRNA表达水平从卵巢发育Ⅱ-Ⅴ期稳步上升,Ⅴ期时达到最高值,Ⅵ期时下降显著且表达水平最低(P < 0.05)(张金勇等, 2016)。当前的研究发现,半滑舌鳎PGRMC1基因和蛋白定位在成熟卵母细胞膜上,预示PGMRC1在细胞膜上介导内分泌调控卵母细胞的成熟过程。另外,Western blotting分析PGRMC1分布在牛的生发泡和M Ⅱ期卵母细胞,参与合子原核的形成;在胚胎发育过程中,囊胚期PGRMC1的表达丰富(Luciano et al, 2010);在哺乳动物中,PGRMC1参与调控胚胎发育,但在低等脊椎动物--鱼类中PGRMC1的调控机制未见报道。在本研究中,PGRMC1在具有受精能力的卵母细胞的细胞膜上表达丰富,呈现母源基因的表达特征,由此推测,PGRMC1在半滑舌鳎胚胎发育过程中也可能具有重要的生理功能。
半滑舌鳎PGRMC1蛋白和mRNA定位在其肝脏组织的胆小管和肝静脉区域,可能因为胆小管和肝静脉的管腔中分布着很多的微绒毛,其上的细胞膜丰富,因此,PGRMC1有明显的杂交信号。半滑舌鳎PGRMC1在肝脏胆小管和肝静脉等与外界联系的管腔周围内细胞有明显的阳性信号,这与已有的鼠PGRMC1的研究结果相一致(Nölte et al, 2000)。
本研究探明了PGRMC1蛋白和mRNA在繁殖相关组织的细胞学定位特征,但关于PGRMC1的具体生理功能作用途径及机制尚不明了,如何解析这些问题需今后更深入的研究。
| Bryan MB, Chung-Davidson YW, Ren JF, et al. Evidence that progestins play an important role in spermiation and pheromone production in male sea lamprey (Petromyzon marinus). General and Comparative Endocrinology , 2015, 212 : 17-27 DOI:10.1016/j.ygcen.2015.01.008 | |
| Dode MAN, Dufort I, Massicotte L, et al. Quantitative expression of candidate genes for developmental competence in bovine two-cell embryos. Molecular Reproduction and Development , 2006, 73 (3) : 288-297 DOI:10.1002/(ISSN)1098-2795 | |
| Hughes AL, Powell DW, Bard M, et al. Dap1/PGRMC1 binds and regulates cytochrome P450 enzymes. Cell Metabolism , 2007, 5 (2) : 143-149 DOI:10.1016/j.cmet.2006.12.009 | |
| Liu L, Wang J, Zhao L, et al. Progesterone increases rat neural progenitor cell cycle gene expression and proliferation via extracellularly regulated kinase and progesterone receptor membrane components 1 and 2. Endocrinology , 2009, 150 (7) : 3186-3196 DOI:10.1210/en.2008-1447 | |
| Lodde V, Peluso JJ. A novel role for progesterone and progesterone receptor membrane component 1 in regulating spindle microtubule stability during rat and human ovarian cell mitosis. Biology of Reproduction , 2011, 84 (4) : 715-722 DOI:10.1095/biolreprod.110.088385 | |
| Lösel RM, Besong D, Peluso JJ, et al. Progesterone receptor membrane component 1-Many tasks for a versatile protein. Steroids , 2008, 73 (9-10) : 929-934 DOI:10.1016/j.steroids.2007.12.017 | |
| Luciano AM, Lodde V, Franciosi F, et al. Progesterone receptor membrane component 1 expression and putative function in bovine oocyte maturation, fertilization, and early embryonic development. Reproduction , 2010, 140 (5) : 663-672 DOI:10.1530/REP-10-0218 | |
| Mansouri MR, Schuster J, Badhai J, et al. Alterations in the expression, structure and function of progesterone receptor membrane component-1 (PGRMC1) in premature ovarian failure. Human Molecular Genetics , 2008, 17 (23) : 3776-3783 DOI:10.1093/hmg/ddn274 | |
| Mourot B, Nguyen T, Fostier A, et al. Two unrelated putative membrane bound progestin receptors, progesterone membrane receptor component 1 (PGRMC1) and membrane progestin receptor (mPR) beta, are expressed in the rainbow trout oocyte and exhibit similar ovarian expression patterns. Reproductive Biology and Endocrinology , 2006, 4 (1) : 1-14 DOI:10.1186/1477-7827-4-1 | |
| Nölte I, Jeckel D, Wieland FT, et al. Localization and topology of ratp28, a member of a novel family of putative steroid-binding proteins. Biochimica Et Biophysica Acta , 2000, 1543 (1) : 123-130 DOI:10.1016/S0167-4838(00)00188-6 | |
| Peluso JJ, Lodde V, Liu X. Progesterone regulation of progesterone receptor membrane component 1 (PGRMC1) sumoylation and transcriptional activity in spontaneously immortalized granulosa cells. Endocrinology , 2012, 153 (8) : 3929-3939 DOI:10.1210/en.2011-2096 | |
| Peluso JJ, Romak J, Liu X. Progesterone receptor membrane component-1 (PGRMC1) is the mediator of progesterone's antiapoptotic action in spontaneously immortalized granulosa cells as revealed by PGRMC1 small interfering ribonucleic acid treatment and functional analysis of PGRMC1 mutations. Endocrinology , 2008, 149 (2) : 534-543 DOI:10.1210/en.2007-1050 | |
| Preechaphol R, Klinbunga S, Yamano K, et al. Molecular cloning and expression of progestin membrane receptor component 1(PGRMC1) of the giant tiger shrimp Penaeus monodon. General and Comparative Endocrinology , 2010, 168 (3) : 440-449 DOI:10.1016/j.ygcen.2010.06.002 | |
| Suchanek M, Radzikowska A, Thiele C. Photo-leucine and photo-methionine allow identification of protein-protein interactions in living cells. Nature Methods , 2005, 2 (4) : 261-267 DOI:10.1038/nmeth752 | |
| Zhang JY, Liu XZ, Shi B, et al. Molecular cloning, tissue and spatio-temporal expression pattern of PGRMC1 in the half-smooth tongue sole (Cynoglossus semilaevis). Journal of Fishery Sciences of China , 2016, 23 (5) : 1080-1090 [张金勇, 柳学周, 史宝, 等. 半滑舌鳎孕酮受体膜组分1基因的克隆及组织和时空表达规律. 中国水产科学 , 2016, 23 (5) : 1080-1090] | |
| Zhang Y, Ruan XY, Tian XX, et al. Progress in research on possible role of progesterone receptor membrane component 1 (PGRMC1) in the mechanism of breast cancer development. Journal of Capital Medical University , 2013, 34 (4) : 496-500 [张颖, 阮祥燕, 田玄玄, 等. 孕激素受体膜组分1 (PGRMC1)在乳腺癌发生风险方面的研究进展. 首都医科大学学报 , 2013, 34 (4) : 496-500] |



