2. 农业部海洋渔业可持续发展重点实验室中国水产科学研究院黄海水产研究所 青岛 266071;
3. 大连海洋大学水产与生命学院 大连 110623
2. Key Laboratory of Sustainable Development of Marine Fisheries, Ministry of Agriculture, Yellow Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Qingdao 266071 ;
3. College of Fisheries and Life Science, Dalian Ocean University, Dalian 116023
鼠尾藻(Sargassum thunbergii)隶属褐藻门、墨角藻目、马尾藻科、马尾藻属,是我国沿海地区重要经济藻类之一(吴海一等, 2010)。鼠尾藻具有胶体成分少的特点,做成的海参饲料对水体污染小,是理想的海参饲料制造原料之一(邹吉新等, 2005)。近年来,随着海参养殖业的快速发展,对鼠尾藻的需求逐年增加,过度的采摘对野生鼠尾藻资源构成了严重的威胁(韩晓弟等, 2005)。目前,国内已有多家科研单位相继展开了鼠尾藻的研究,主要集中于生物学(王志芳等, 2008; 宋广军等, 2011; Chu et al, 2011; 邵魁双等, 2010; 张泽宇等, 2007)、人工育苗(孙修涛等, 2010; 詹冬梅等, 2006; 李美真等, 2009; 王增福等, 2007)、遗传多样性(Zhao et al, 2007; 刘玮等, 2011; 伊新华等, 2010)及藻类生理特性(梁洲瑞等, 2011a、b; 姜宏波等, 2005、2009)。
桑沟湾是北方重要的贝、藻养殖基地,藻类养殖以海带(Saccharina japonica)为主,每年4-7月为海带的收获期,海区有较多的空闲筏架。鼠尾藻生长适宜温度为9.6-19.8℃(邹吉新等, 2005),在桑沟湾海区满足该温度区间的时间为4月中下旬至7月上旬。因此,在桑沟湾开展鼠尾藻养殖,一方面能充分利用养殖设施资源,另一方面通过鼠尾藻养殖可改善养殖海区生态环境。本文通过研究鼠尾藻在桑沟湾的生长特性,旨在为桑沟湾鼠尾藻人工养殖的开展提供理论依据。
桑沟湾养殖海区附着生物种类多、数量大(齐占会等, 2010)。过多的附着生物可能会影响鼠尾藻的生长及品质,其潜在的影响不容忽视。筏式养殖鼠尾藻的附着生物虽有报道(邹吉新等, 2005; 原永党等, 2006),但对附着生物的群落结构缺乏系统的研究。本实验对桑沟湾鼠尾藻养殖过程中出现的附着生物群落结构进行了研究,旨在阐明鼠尾藻养殖过程中附着生物的种类、数量月份变化规律,为污损生物的防除提供理论依据。
1 材料与方法 1.1 材料实验所用鼠尾藻苗种为2014年4月中旬购买于浙江省温州市洞头县的野生种野生苗种。苗种装入聚乙烯编织袋(100 cm×50 cm),每个袋子装苗15 kg,同时放入海水冰瓶冷却,经24 h长途运输,到达山东省荣成市楮岛水产有限公司,于次日悬挂于桑沟湾海区进行养殖。养殖海区水深为6-8 m,实验海区面积为666.67 m2。
1.2 方法鼠尾藻是潮间带耐强光藻类,4000lx以上光强更有利于藻体侧枝的生长(孙修涛等, 2006),藻体适合浅水层养殖。故本研究采用平养方式进行养殖,即将苗绳两端分别挂于两行筏架上,利用藻体自身浮力使藻体悬浮于海区表层。所用苗绳为聚乙烯绳,长度为3 m,直径为0.5 cm。夹苗时3-4支鼠尾藻为一簇,每绳夹苗60簇。分枝4支以下的鼠尾藻连同盘状固着器一起夹于苗绳上,分枝4支以上的则保留4支分枝,其余剪下夹到其他苗绳上。666.67m2实验海区共养殖鼠尾藻300绳。
在实验期间,每隔10d采集1次样品,每次采样30支,剥离附着生物后,测量藻体主枝长度、湿重、生殖托长度,同时测定所剥离附着生物的湿重。测量结束后,用70%乙醇固定附着生物样品,保存于4℃的冰箱,以备分类鉴定。鼠尾藻藻体则置于60℃烘箱里烘干48 h,测量藻体干重。用YSI-Pro10(美国)测定海区环境因子(水温、溶解氧、盐度和pH)。采集水样,按照《海洋监测规范》(GB17378-2007)的要求进行分析,分别采用次溴酸钠氧化法、锌-镉还原法和重氮偶氮法测定NH4-N、NO3-N和NO2-N,采用磷钼蓝法测定PO4-P。总溶解无机氮(DIN)浓度为NH4-N、NO3-N和NO2-N浓度之和。
1.3 计算方法鼠尾藻干湿比为藻体干重与湿重的比值。特定生长率按如下公式计算:
特定生长率(Specific growth rate SGR, %/d)
=(lnmt-lnm0)/t×100%
式中, m0为初始藻的鲜重量(g);mt为实验结束时藻的鲜重量(g);t为实验持续的天数。
1.4 数据处理采用Excel整理数据及绘制图表,数据用平均值±标准差(Mean±SD)形式表示。
2 结果与分析 2.1 桑沟湾养殖海区环境因子变化海区环境因子变化见表 1。从表 1可以看出,4月21日海水温度为10.4℃,随后呈逐步上升趋势,每隔6-7 d水温上升1℃,6月24日水温超过20℃。溶氧变化区间为7.15-9.78 mg/L。盐度保持在31左右。海区pH在8.01-8.26之间变化。DIN浓度在4.17-14.86 mmol/L之间, PO4-P浓度在0.20-1.23 mmol/L之间。
|
|
表 1 实验海区水温、溶解氧、盐度、pH、DIN、PO4-P的变化 Table 1 Variations in the temperature, dissolved oxygen, salinity, pH, DIN and PO4-P in the experimental area. |
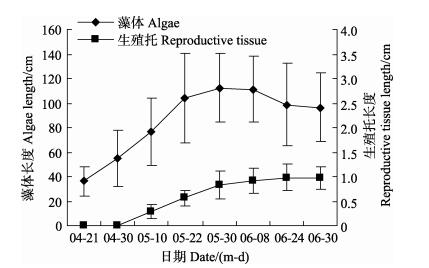
鼠尾藻藻体长度变化见图 1。从图 1可以看出,4月21日-5月30日期间,藻体呈现快速生长趋势,日增长比例达到2.79%,而5月30日-至6月30日为-0.47%,呈下降趋势。养殖期间,藻体长度最大值平均为(112.31±27.93) cm。
|
图 1 鼠尾藻藻体与生殖托长度的变化 Figure 1 Changes in the algae length and reproductive tissue length of S. thunbergii |
生殖托直至5月10日以后才少量出现,随后长度呈持续增长趋势(图 1),且出现生殖托藻体的比例也持续增大。藻体生长至6月24日,大部分生殖托上的生殖孔明显打开,部分藻体完成精卵的排放。
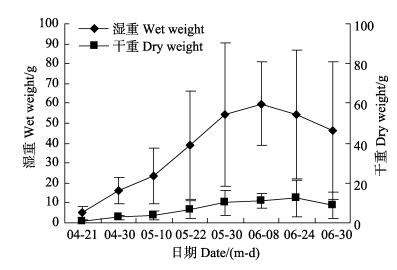
鼠尾藻湿重在4月21日-5月30日期间呈现持续快速增长趋势,6月8日达到最大值,随后开始下降(图 2)。单株藻体重量最大值平均为(59.78±20.86) g。
|
图 2 单株鼠尾藻平均干重与湿重的变化 Figure 2 Changes in the wet weight and dry weight of individual S. thunbergii |
鼠尾藻干重在4月21日-6月24日期间呈现上升趋势,直至6月24日达到最大值,之后随着藻体湿重变化也呈现下降趋势(图 2)。
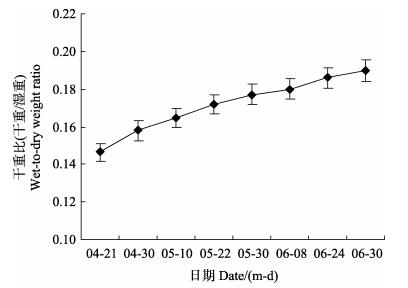
鼠尾藻干湿比呈现上升趋势,由0.146(4月21日)上升至0.190(6月30日)(图 3)。
|
图 3 鼠尾藻平均干湿比的变化 Figure 3 Changes in the wet-to-dry weight ratio of S. thunbergii |
6月24日,鼠尾藻生物量最大时,统计掉苗率为10.3%。测量藻体根部直径为(0.18±0.03) cm。
鼠尾藻养殖在10-49 d期间,湿重增长迅速,其SGR呈先上升后下降趋势(表 2)。SGR与水温(T, ℃)之间的拟合相关方程为
| $ SCR = - 0.44{T^2} + 13.15T - 93.93 \times 100\% \left({{R^2} = 0.8375} \right) $ |
|
|
表 2 鼠尾藻SGR与水温变化 Table 2 Changes in the specific growth rate and temperature |
结果显示,鼠尾藻藻体上的附着生物群落结构复杂,附着生物种类包括藻类、海鞘类、环节动物、腔肠动物、软体动物、甲壳动物和海绵动物。共鉴定大型附着生物16种(表 3)。
|
|
表 3 4-6月鼠尾藻藻体上大型附着生物种类 Table 3 Macro-fouling species on the surface of S. thunbergiifrom April to June |
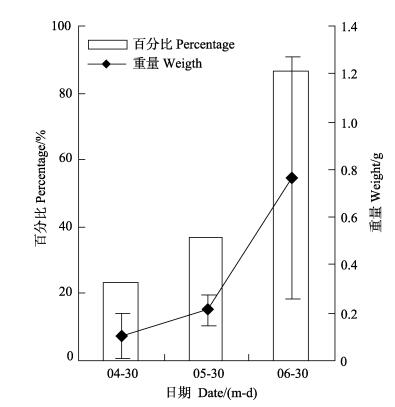
鼠尾藻养殖前期(4月),附着生物种类只有4种,单株藻体上附着生物量平均为(0.10±0.09) g。随着水温的升高及鼠尾藻的生物量的增大,可供附着的面积增大,附着生物的种类及生物量随之增加(图 4)。5月30日,附着生物种类达到8种,单株藻体上附着生物量均值达到(0.21±0.07) g。6月30日附着生物达到16种,每株藻体上附着生物量均值达到(0.77±0.51) g。6月30日,尖嘴扁颌针鱼(Ablennes anastomella)鱼卵是附着生物的主要构成种类,其次是海鞘类与海绵动物,随机调查的30株藻体上共计发现尖嘴扁颌针鱼鱼卵600粒,预计666.67 m2实验海区鱼卵可达126万粒。
|
图 4 单株藻体上附着生物的平均湿重及出现附着生物的鼠尾藻百分比的变化 Figure 4 Changes in the wet weight of biofouling and the percentage on S. thunbergii carrying biofouling |
温度对鼠尾藻的生理(孙修涛等, 2006)、生长(包杰等, 2008)有显著的影响,水温成为鼠尾藻养殖的限制因子。通常情况下,海水温度为10-20℃的月份为鼠尾藻的养殖期(表 4)。在浙江温州海区适合鼠尾藻生长的时间为2-5月(权伟等, 2014),在山东威海海区适合鼠尾藻生长的时间为3-7月(原永党等, 2006),在大连海区适合鼠尾藻生长的时间为4-11月(王丽梅等, 2011)。因此,从鼠尾藻养殖生长期来看,应选择夏季最高温度不超过20℃的海区。本研究拟合得到SGR与水温的相关函数方程为
| $ SGR = - 0.44{T^2} + 13.15T - 93.93\left({{R^2} = 0.8375} \right) $ |
依据函数所得到最佳生长温度为14.9℃。詹冬梅等(2013)研究发现海上养殖鼠尾藻长度增加最快的温度为15-16℃。孙修涛等(2006)研究了鼠尾藻新生枝条的适宜温度为16℃。这表明温度在15℃左右,鼠尾藻的生长处于最佳状态。鼠尾藻适宜生长温度为10-20℃,温度超过20℃时,藻体生物量发生衰亡(表 4),这与本研究结果相一致。在鼠尾藻养殖过程的中后期,应加强对水温变化的关注并及时观察鼠尾藻的性成熟情况。当水温超过20℃或者大部分藻体生殖孔打开时,应对鼠尾藻进行采收。
鼠尾藻养殖方式也会对它的产量有较大的影响。王丽梅等(2011)研究表明,使用海带绳夹苗所养出来鼠尾藻的长度,要低于使用聚乙烯绳。较重的苗绳,使得养殖绳不易保持水平,向下倾斜,对喜阳性鼠尾藻的生长并不利。本研究所采用藻苗为南方大规格苗,所用苗绳直径为0.5 cm的轻质聚乙烯绳,鼠尾藻自身的浮力较大(鼠尾藻气囊发达),并不存在苗绳向下倾斜的问题。因此,在鼠尾藻气囊未长出前,应注意养殖绳所处的水层位置,避免水层过深而影响鼠尾藻的生长。此外,营养盐、pH等其他环境理化因子可能对鼠尾藻的产量有影响,仍需进一步研究探索。
桑沟湾是我国重要的贝、藻养殖基地,研究表明,桑沟湾理化因子稳定,满足鼠尾藻生殖托(马兴宇等, 2013)、藻体(丁刚等, 2014)快速生长的需求。本研究表明,每公顷实验海区共收获藻体湿重为43.95 t,产量要高于其他研究结果(表 4),鼠尾藻适宜在桑沟湾养殖。按照3元/kg(鲜重)的单价,预计每公顷产值约为13万元,除去苗种等成本,效益可达6万元左右。因此,在桑沟湾大规模开展鼠尾藻养殖的可行的。
|
|
表 4 鼠尾藻不同区域的生长特性 Table 4 Growth characteristics of S. thunbergii in different areas |
温度是影响生物群落特征的最重要因素(Lodeiros et al, 2000)。在鼠尾藻养殖期间,水温从10.4℃上升至21.4℃,附着生物的生物量也呈现上升趋势。齐占会等(2010)研究表明,桑沟湾海区附着生物的生物量随温度上升而增加,这与本研究的结果相一致。
本研究结果显示,在桑沟湾养殖鼠尾藻,主要附着生物为尖嘴扁颌针鱼鱼卵、玻璃海鞘、强壮藻钩虾(Ampithoe valida)、马尾藻。邹吉新等(2005)研究结果是大量贻贝(Mytilus edulis)附着;原永党等(2006)研究结果表明,附着生物则是贻贝、麦秆虫(Caprellap sp.)和钩虾。不同的地域之间,环境理化因子不同,导致附着生物群落的生物种类不同,东海的污损生物优势种与黄、渤海明显不同(严涛等, 2008)。尖嘴扁颌针鱼为暖水性凶猛上层鱼类,生活在近海浅水水域,每年5-6月在沿海各海域均能产卵。本研究发现,桑沟湾人工养殖鼠尾藻附着生物中,尖嘴扁颌针鱼鱼卵占据了较大的生物量比例,发现的鱼卵预计达126万粒,说明人工养殖条件下鼠尾藻藻场是尖嘴扁颌针鱼理想的排卵场所,但过多的鱼卵可能会影响鼠尾藻的品质。一般情况下,海水温度上升至20℃之前,就要对鼠尾藻进行采收,而在这个温度之前,海区并不会暴发式地出现附着生物(齐占会等, 2010),因此,鼠尾藻生长受附着生物的影响较小。
实验结束时,666.67 m2实验海区共收获鼠尾藻藻体湿重2.93 t,估算附着生物共4.83 kg,附着生物占鼠尾藻总湿重0.16%,对鼠尾藻成品品质影响不大。但是掉苗率是否与附着生物有关,仍需进一步研究。
3.3 存在的问题鼠尾藻养殖中后期藻体湿重生长不明显。4月21日-5月30日藻体湿重SGR为6.1%,5月30日-6月24日藻体湿重SGR为0.49%。5月30日每绳鼠尾藻藻体已达12.14kg,藻体相互缠绕覆盖,所采集的样品、藻体颜色出现明显的异常,裸露在外部的藻体呈现黄褐色,覆盖在内部的藻体呈现黑褐色,其原因可能是密度制约所引起的光线不足、缺氧、水体交换不足。胡凡光等(2013a)在鼠尾藻养殖研究中也出现了藻体由褐色变成黑褐色的现象,造成这种现象的原因可能是光照减弱,主要归因于养殖方式问题,筏架设施、水流与挂苗方式存在着一些不足,需要进一步改进。
本研究结束时,藻体掉苗率为10.3%。原因一方面是鼠尾藻根部过细。经过90 d的养殖,鼠尾藻根部仍然很细,6月30日收获的样品,直径为(0.18±0.03) cm,过细的根部可能会导致鼠尾藻掉苗现象;另一方面,海区风浪因素。如何降低鼠尾藻掉苗率问题,仍需进一步深入研究。
| 丁刚, 于晓清, 詹冬梅, 等. 不同氮、磷浓度及配比对鼠尾藻幼苗生长的影响. 水产科学 , 2014, 33 (4) : 219-222 | |
| 马兴宇, 梁洲瑞, 刘福利, 等. 环境因子对鼠尾藻生殖托生长及光合特性的影响. 中国水产科学 , 2013, 20 (4) : 851-858 | |
| 王志芳, 张全胜, 潘金华. 烟台芦洋湾鼠尾藻种群生物量结构的季节变化. 中国水产科学 , 2008, 15 (6) : 992-998 | |
| 王丽梅, 宋广军, 何平, 等. 鼠尾藻人工苗种保苗及海上养殖技术研究. 渔业现代化 , 2011, 38 (4) : 37-40 | |
| 王增福, 刘建国. 鼠尾藻(Sargassum thunbergii)有性生殖过程与育苗. 海洋与湖沼 , 2007, 38 (5) : 453-457 | |
| 包杰, 田相利, 董双林, 等. 温度、盐度和光照强度对鼠尾藻氮、磷吸收的影响. 中国水产科学 , 2008, 15 (2) : 293-300 | |
| 刘玮, 李美真, 吴海一, 等. 我国沿海鼠尾藻(Sargassum thunbergii)遗传资源RAPD分析. 海洋与湖沼 , 2011, 42 (4) : 608-611 | |
| 李美真, 丁刚, 詹冬梅, 等. 北方海区鼠尾藻大规格苗种提前育成技术. 渔业科学进展 , 2009, 30 (5) : 75-82 | |
| 齐占会, 方建光, 张继红, 等. 桑沟湾贝藻养殖区附着生物群落季节演替研究. 渔业科学进展 , 2010, 31 (4) : 72-77 | |
| 权伟, 应苗苗, 康华靖, 等. 不同野生种源鼠尾藻生长及固碳速率. 中国农学通报 , 2014, 30 (5) : 79-82 | |
| 邵魁双, 巩宁, 王金霞, 等. 鼠尾藻种群生态学研究. 海洋环境科学 , 2010, 29 (3) : 332-336 | |
| 宋广军, 王丽梅, 李世国, 等. 大连沿海野生鼠尾藻种群生态调查. 水产科学 , 2011, 30 (9) : 527-532 | |
| 孙修涛, 王飞久, 汪文俊, 等. 基于有性繁殖的鼠尾藻规模化繁育试验. 渔业科学进展 , 2010, 31 (3) : 84-91 | |
| 孙修涛, 王飞久, 刘桂珍. 鼠尾藻新生枝条的室内培养及条件优化. 渔业科学进展 , 2006, 27 (5) : 7-12 | |
| 吴海一, 刘洪军, 詹冬梅, 等. 鼠尾藻研究与利用现状. 国土与自然资源研究 , 2010 (1) : 95-96 | |
| 严涛, 曹文浩. 黄、渤海污损生物生态特点及研究展望. 海洋学研究 , 2008, 26 (3) : 107-118 | |
| 伊新华, 李世国, 何平, 等. 6个野生鼠尾藻种群遗传多样性的AFLP分析. 中国水产科学 , 2010, 17 (5) : 922-929 | |
| 张泽宇, 李晓丽, 韩余香, 等. 鼠尾藻的繁殖生物学及人工育苗的初步研究. 大连水产学院学报 , 2007, 22 (4) : 255-259 | |
| 邹吉新, 李源强, 刘雨新, 等. 鼠尾藻的生物学特性及筏式养殖技术研究. 齐鲁渔业 , 2005, 22 (3) : 25-28 | |
| 胡凡光, 王志刚, 李美真, 等. 鼠尾藻池塘秋冬季栽培生态观察. 渔业科学进展 , 2013a, 34 (1) : 151-158 | |
| 胡凡光, 王志刚, 李美真, 等. 鼠尾藻池塘栽培生态观察. 渔业科学进展 , 2013b, 34 (6) : 124-132 | |
| 姜宏波, 田相利, 董双林, 等. 温度和光照强度对鼠尾藻生长和生化组成的影响. 应用生态学报 , 2009, 20 (1) : 185-189 | |
| 姜宏波, 田相利, 董双林, 等. 不同营养盐因子对鼠尾藻氮、磷吸收速率的影响. 中国海洋大学学报 , 2005, 37 (S1) : 175-180 | |
| 原永党, 张少华, 孙爱凤, 等. 鼠尾藻劈叉筏式养殖试验. 海洋湖沼通报 , 2006 (2) : 125-128 | |
| 梁洲瑞, 王飞久, 孙修涛, 等. 环境因子对鼠尾藻幼苗叶绿素荧光参数的影响. 水产学报 , 2011a, 35 (8) : 1225-1232 | |
| 梁洲瑞, 王飞久, 孙修涛, 等. 利用叶绿素荧光技术揭示光照、温度和盐度对鼠尾藻嫩芽的影响. 海洋科学 , 2011b, 35 (12) : 21-27 | |
| 韩晓弟, 李岚萍. 鼠尾藻特征特性与利用. 特种经济动植物 , 2005, 8 (1) : 27 | |
| 詹冬梅, 李美真, 丁刚, 等. 鼠尾藻有性繁育及人工育苗技术的初步研究. 渔业科学进展 , 2006, 27 (6) : 55-59 | |
| 詹冬梅, 刘梦侠, 李翘楚, 等. 温度对室内鼠尾藻生长影响及海上快速养殖试验. 海洋湖沼通报 , 2013 (3) : 63-66 | |
| Chu SH, Zhang QS, Liu SK, et al. Trade-off between vegetative regeneration and sexual reproduction of Sargassum thunbergii. Hydrobiologia , 2011, 678 (1) : 127-135 DOI:10.1007/s10750-011-0835-9 | |
| Lodeiros CJM, Himmelman JH. Identification of factors affecting growth and survival of the tropical scallop Euvola (Pecten) ziczac in the Golfo de Cariaco, Venezuela. Aquaculture , 2000, 182 (1-2) : 91-114 DOI:10.1016/S0044-8486(99)00245-8 | |
| Zhao FJ, Wang XL, Liu JD, et al. Population genetic structure of Sargassum thunbergii (Fucales, Phaeophyta) detected by RAPD and ISSR markers. J Appl Phycol , 2007, 19 (5) : 409-416 DOI:10.1007/s10811-006-9147-2 |



